今天是2018年9月3日
农历七月二十四
医麦客:CAR-T治疗霍奇金淋巴瘤
2018年9月3日/医麦客 eMedClub/--2018年1月31日,《Science Translational Medicine》报道:来自斯坦福大学医学院的免疫学大牛Ronald Levy及其研究团队开发出一种新型治疗方式(癌症疫苗:TLR9激动剂+抗OX40抗体+放疗),能够有效消除小鼠体内所有的癌症痕迹!甚至包括远端未经处理的转移病灶!
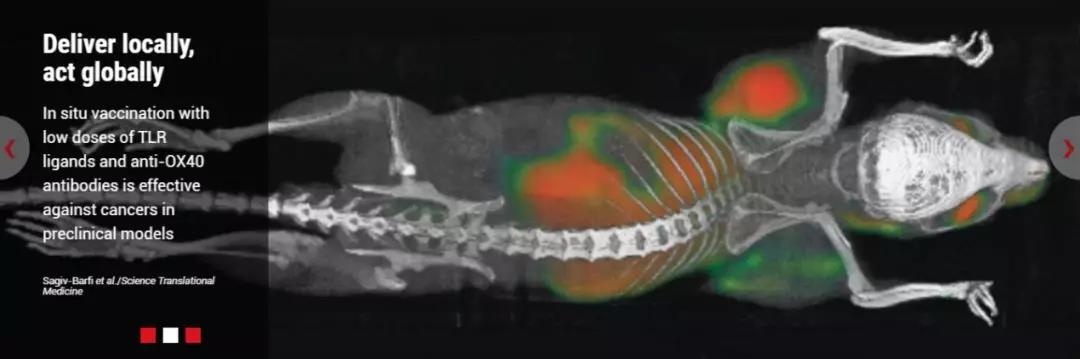
Science Translational Medicine
当时,这一研究成果引起了肿瘤免疫学领域的轩然大波,相关新闻报道成刷屏模式。
目前,相关临床试验(NCT03410901)正在招募患者,以评估TLR9激动剂SD-101与抗OX40抗体BMS 986178以及放射疗法一起使用治疗低级别B细胞非霍奇金淋巴瘤的安全性与有效性。
推荐阅读:
振奋人心! 斯坦福免疫大牛开发的新型癌症疫苗让90只小鼠全部显示无癌!现已进入临床试验阶段丨医麦黑科技
而我们今天要说的就是,这款新型癌症疫苗中的TLR9激动剂,肿瘤免疫治疗领域的黑马角色!
TLR9激动剂
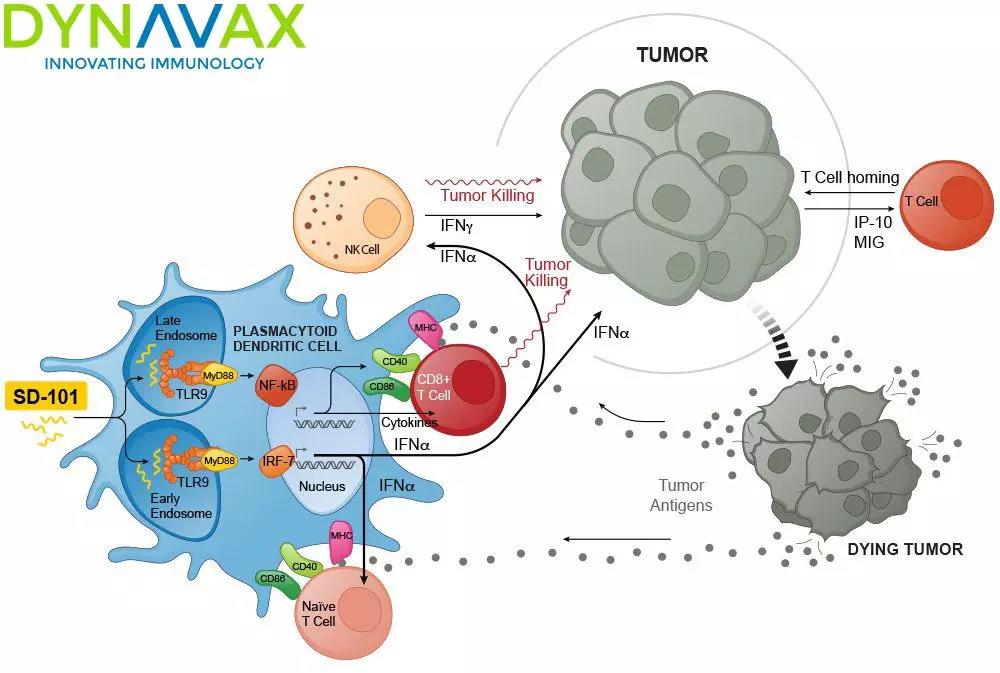
TLR9激动剂SD-101作用机制(图片来源 Dynavax)
以Dynavax公司在研的SD-101为例,我们先来了解TLR9激动剂的作用机制,其高效激活两种主要的TLR9信号传导通路:
1. 第一个通路导致IFN-α的快速产生,进而激活自然杀伤细胞,阻断免疫抑制,以及促进Th1和CD8 + T细胞归巢到肿瘤中。
2. 第二个通路导致肿瘤特异性细胞毒性CD8 + T细胞的有效产生和活化。
另外,SD-101直接注射至肿瘤内,可以聚焦TLR9刺激相关的癌症杀伤活性,同时还有高浓度肿瘤细胞死亡后的特异性抗原。这种对特异性肿瘤抗原的暴露可以产生记忆T细胞,产生长期的免疫治疗作用(和疫苗的机制类似)。

近日,Dynavax公司宣布,两篇同行评审的SD-101临床研究报告已发表在权威学术期刊《Cancer Discovery》上。其中一篇论文是Ronald Levy博士领导的TLR 9激动剂原位免疫接种治疗淋巴瘤的临床试验,另一片论文是Antoni Ribas博士领导的TLR 9激动剂联合PD-1抗体Keytruda治疗黑色素瘤的临床试验。
TLR 9激动剂原位原位接种疫苗

左为癌症免疫疗法领域的先驱 Ronald Levy博士(图片来源 斯坦福医学院)
这项由Ronald Levy博士领导的多中心1/2期临床试验旨在评估瘤内注射TLR9激动剂SD-101联合低剂量放射治疗未经治的惰性淋巴瘤患者瘤患者的安全性和有效性。
临床试验结果显示:29名可评估的患者在接受该联合疗法后,未发生与治疗相关的4级或严重不良事件,而且几乎所有患者治疗部位的肿瘤都发生了缩小。更重要的是,24名患者未经治疗部位的肿瘤也获得了显著缩小,5名患者获得部分缓解PR,1名患者获得完全缓解CR。
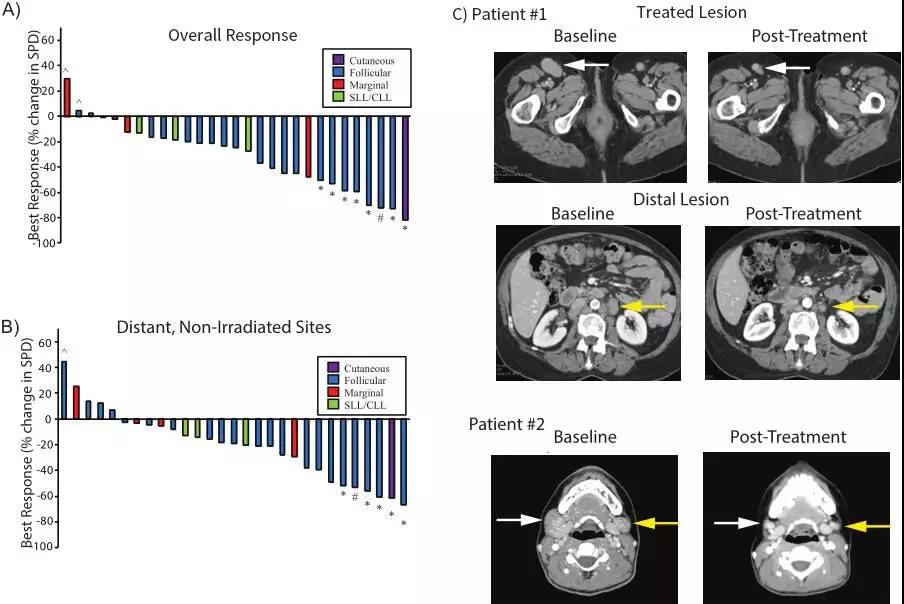
SD-101联合低剂量放疗诱导患者肿瘤免疫应答(图片来源 cancerdiscovery)
与此同时,研究人员在肿瘤微环境中观察到治疗相关的CD8 +和CD4 +效应T细胞的增加以及滤泡辅助T细胞和调节性T细胞(Treg)的减少。而低预处理水平的CD4 + Tregs、增殖的CD8 + T细胞和GranzymeB + CD8 + T细胞与良好的临床结果相关。
总而言之,瘤内注射TLR 9激动剂SD-101联合低剂量放疗的耐受性良好,能够导致治疗部位和未经治疗疾病部位的肿瘤消退。
TLR 9激动剂联合PD-1抗体

Antoni Ribas博士(图片来源 cancer.gov)
由Antoni Ribas博士领导1b期多中心临床研究,旨在评估TLR 9激动剂SD-101联合PD-1抗体Keytruda(Pembrolizumab)肿瘤不可切除或转移性恶性黑色素瘤患者的安全性和有效性。
临床结果显示:22名患者接受该组合治疗,耐受性良好。与SD-101相关的最常见不良事件是短暂的注射部位反应,轻度至中度的“流感样”症状。
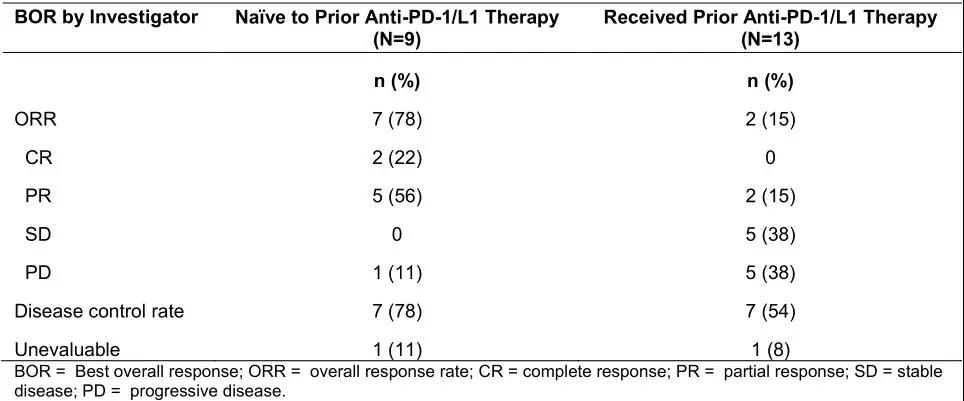
临床试验结果(图片来源 cancerdiscovery)
在外周和内脏病变中均观察到了持久的肿瘤免疫应答。在9例未接受抗PD-1治疗的患者中,总体有效率(ORR)为78%。预估12个月无进展生存期(PFS)率为88%,总生存期(OS)率为89%。在先前接受过抗PD-1抗体治疗的13名患者中,ORR为15%。
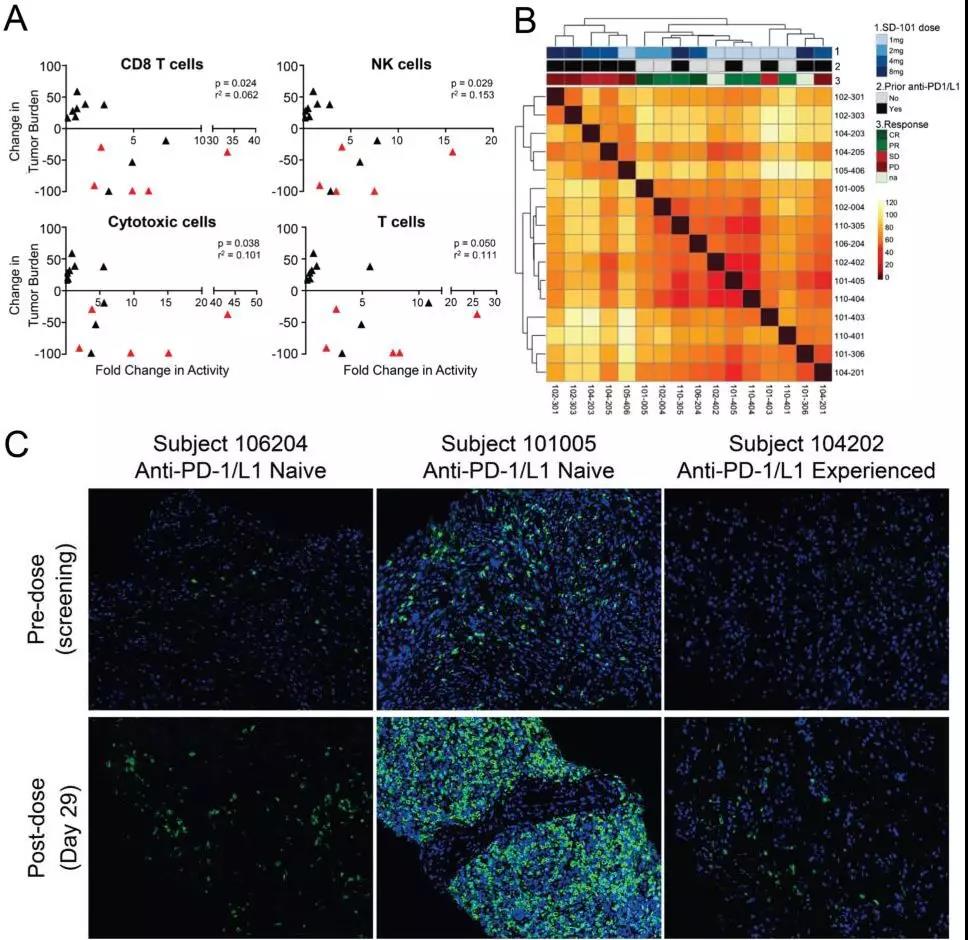
肿瘤微环境中药效学的变化(图片来源 cancerdiscovery)
与此同时,生物标志物数据也支持这些临床结果,其在肿瘤微环境中诱导了广泛的免疫激活,包括增加NK细胞、细胞毒性细胞、树突细胞、B细胞和CD8 + T细胞以及T细胞浸润,而CD4 +和CD8 + T细胞的增加通常与肿瘤免疫应答相关。
推荐阅读:
免疫联合疗法领域再现黑马,实力逆转冷热肿瘤,挑战PD-1/L1抗体耐药怪圈丨医麦猛爆料
另外,值得一提的是,在2018年AACR年会上,CMP-001(TLR9激动剂)也成功了的引起了行业内的关注。I期临床数据显示,CMP-001联合PD-1抗体治疗PD-1无效或者耐药的患者,有效率高达22%,其中部分患者肿瘤完全消失。实力逆转冷热肿瘤,挑战PD-1/L1抗体耐药怪圈。
综上所述,肿瘤内注射TLR9激动剂的多项临床前及临床试验都提供了极具说服力的研究数据,表明通过TLR9途径刺激先天免疫系统可以增强注射和非注射部位肿瘤的适应性免疫反应。作为癌症免疫疗法的联合对象,其潜力不可估量,还有待于进一步发掘。
参考出处:
https://finance.yahoo.com/news/dynavax-announces-publication-two-papers-103000704.html
https://med.stanford.edu/news/all-news/2018/01/cancer-vaccine-eliminates-tumors-in-mice.html
http://cancerdiscovery.aacrjournals.org/content/early/2018/08/24/2159-8290.CD-18-0743
http://cancerdiscovery.aacrjournals.org/content/early/2018/08/24/2159-8290.CD-18-0280
本文系转载,来源于医麦客


